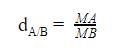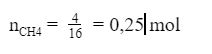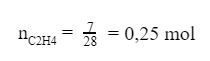Làm sao để biết được chất khí nào đó có những tính chất gì? Làm thế nào để chúng ta biết được chất khí đó nhẹ hay nặng hơn khí Hidro H2, khí Oxi O2 hay không khí. Vậy câu hỏi đặt ra là: Tỉ khối chất khí là gì? Tỉ khối của không khí? Công thức nào được áp dụng để tính tỉ khối của chất khí? Làm sao tính được tỉ khối so với không khí, với khí Oxi hay so với khí Hidro? Tất cả câu hỏi trên sẽ được giải đáp qua bài sau.
Đang xem: Tỉ khối là gì, công thức tính tỉ khối hơi và bài tập Điển hình
Tỉ khối của chất khí
Định nghĩa tỉ khối của chất khí
Khái niệm tỉ khối chỉ sử dụng cho chất khí. Tỉ khối của chất khí là công thức giúp xác định phân tử khối của khí A so với khí B, để biết chất khí A nhẹ hay nặng hơn chất khí B bao nhiêu lần. Cách so sánh đó là khối lượng mol của hai chất khí đó với nhau MA và MB.
Công thức tính
Trong đó:
dA/B là tỉ khối giữa khí A với khí BMA là khối lượng mol khí AMB là khối lượng mol khí B

Tỉ khối của chất khí
Khí A nhẹ hay nặng hơn khí B

Công thức xác định khí A nhẹ hay nặng hơn khí B

Khí A nhẹ hay nặng hơn khí B
Lưu ý:
Nếu dA/B Nếu dA/B = 1 suy ra khí A bằng hơn khí BNếu dA/B > 1 suy ra khí A lớn hơn khí B
Khí A nhẹ hay nặng hơn không khí
Không khí trong thực tế là hỗn hợp của nhiều khí khác nhau, để đơn giản trong tính toán, ta xem không khí gồm 20% khí oxi và 80% khí nito. Khối lượng mol không khí (tức 1 mol không khí) được tính như sau:
Khối lượng của 0,2 mol khí oxi + 0,8 mol khí nitơ
MKK = (32 x 0,2) + (28 x 0,8) = 28,8 (g/mol) làm tròn thành 29 (g/mol)
Do đó, để biết khí A này nhẹ hay nặng hơn không khí mấy lần, ta sẽ tiến hành so sánh khối lượng mol của khí A (MA) đối với khối lượng mol không khí (Mkk = 29 g/mol)
Công thức tính tỉ khối chất khí A so với không khí:

Công thức tính tỉ khối chất khí A so với không khí
Trong đó:
dA/KK là tỉ khối giữa khí A với không khíMA là khối lượng mol của khí A29 là khối lượng mol của không khí

Khí A nhẹ hay nặng hơn không khí
Ví dụ: Khí Hidro (H2) nhẹ hay nặng hơn không khí mấy lần?
Tỉ khối của chất khí H2 so với không khí là:

Tỉ khối của chất khí H2 so với không khí
Kết luận: khí Hidro (H2) nhẹ hơn không khí 0,069 lần.
Tỉ khối của hỗn hợp các khí
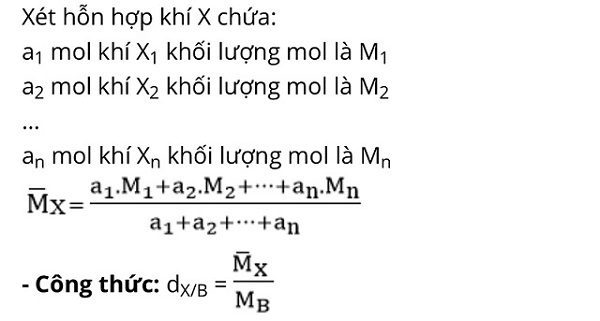
Tỉ khối của hỗn hợp các khí
Tổng kết kiến thức
Qua phần lý thuyết mol tỉ khối của chất khí trên, bạn cần nắm được nội dung sau:
1/ Cách xác định khí A nhẹ hay nặng hơn khí B bao nhiêu lần, công thức tỉ khối giữa khí A và khí B
2/ Cách xác định khí A nhẹ hay nặng hơn không khí bao nhiêu lần, công thức tỉ khối giữa khí A và không khí
3/ Các công thức tính tỉ khối liên quan
Các dạng bài tập hay gặp
Dạng 1: Xác định tỉ khối hỗn hợp khí
Một vài lưu ý cần nhớ:
Bước 1: Trong hỗn hợp khí tính khối lượng mol trung bình
Bước 2: Xác định tỉ khối hỗn hợp khí
Ví dụ 1: Tỉ khối hỗn hợp chứa 7g khí etilen (C2H4) và 4g khí metan (CH4) so với không khí là bao nhiêu?
Hướng dẫn:
Số mol của CH4 là:
Số mol của C2H4 là:
Suy ra hỗn hợp khí có khối lượng trung bình là:
Ví dụ 2: Một hỗn hợp X gồm O2 và H2 (điều kiện không có phản ứng xảy ra), hỗn hợp có tỉ khối đối với không khí là 0,3276. Tính phần trăm theo số mol của H2 trong hỗn hợp.
Xem thêm: Khái Niệm Về 3 Dải Tần Số Âm Treble Là Gì ? Cách Chỉnh Âm Treble Hay Nhất
Hướng dẫn:
Gọi số mol của khí H2 và O2 trong hỗn hợp X lần lượt là x (mol) và y (mol)
Tỉ khối của hỗn hợp X so với không khí là:
Ví dụ 3: Tính tỉ khối hỗn hợp có chứa khí N2 và khí O3 có tỉ lệ tương ứng là 1 : 2 so với không khí.
Hướng dẫn:
Gọi số mol của khí N2 là a mol suy ra số mol của khí O3 là 2a mol
Hỗn hợp khí cần tìm có khối lượng trung bình là:
Ví dụ 1: Tỉ khối của khí A đối với khí B là 2,125 và tỉ khối khí B đối với oxi là 0,5. Tính khối lượng mol của khí A.
Xem thêm: ” Solicit Là Gì ? Nghĩa Của Từ Solicit Trong Tiếng Việt Solicit Là Gì, Nghĩa Của Từ Solicit
Hướng dẫn:
Ta có:
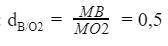
Suy ra MB = 32 x 0,5 = 16
Mặt khác:
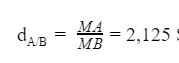
Suy ra MA = 2,125 x 16 = 34
Kết luận: khối lượng mol của khí A là 34 g/mol
Ví dụ 2: Khí X2 có tỉ khối so với khí axetilen (C2H2) là 2,731 g/mol. Tìm khí X2
Hướng dẫn:
Mà = 2 x MX = 71 suy ra MX = 35,5
Vậy khí cần tìm là khí Cl2
Ví dụ 3: Khí A có dạng công thức phân tử là RO2, tỉ khối khí A so với H2 là 32. Tìm công thức phân tử của khí A.
Hướng dẫn:
Theo đầu bài ta có: tỉ khối khí A so với H2 là 32
A có công thức phân tử dạng RO2 suy ra M = MR + 2.MO = 64
=> MR = 64 – 2.16 = 32 vậy R là nguyên tố S
Kết luận: công thức phân tử của khí A là SO2
Bài viết trên đây đã cung cấp cho bạn đọc những kiến thức cơ bản về tỉ khối của chất khí, công thức tính cùng các dạng bài tập hay gặp. Hy vọng bài viết của chúng tôi sẽ giúp bạn học tập và nghiên cứu được nhiều kiến thức. Chúc bạn thành công!